子宮の中の細菌が着床に影響する?
~子宮内細菌叢検査とその原理~
1回目の採卵で、3個胚盤胞を凍結。1個ずつ、2回移植したけれど残念ながら着床せず。
次は3回目の移植、これで凍結胚は最後だからその次はまた採卵か、と思っていたら、「2回着床しなかったので、子宮の中の細菌を調べる検査をする選択肢があります。もし、着床に悪さをする細菌がいたり、必要な細菌が少なかったら、治療することもできますよ」と先生からアドバイスがありました。
え、子宮の中って、検査ができるほど細菌がたくさんいるのかな?子宮の中で受精卵と一緒になっても、感染したりしないの?
子宮内細菌叢検査
形態がとてもよい胚を何回か移植しても着床しないときに、子宮側の要因を考えてもよい場合があります。様々な検査がありますが、代表的な検査に子宮の中にいる細菌の種類を調べる検査(子宮内細菌叢検査;商品名としては、EMMA™、ALICE™、フローラ検査™など)があります。
子宮の中にいる細菌は全体としてごく微量ですが、その中では乳酸菌が割合として多いといわれています(図1a)。この乳酸菌の割合が少なかったり(図1b)、着床を妨げる悪い細菌(病原菌)がいる場合(図1c)には着床率が下がってしまい、本来は妊娠するはずの胚が着床に失敗することがあるといわれています※1。そこで乳酸菌が少ない場合には乳酸菌を増やすお薬を、また着床を妨げる細菌がいる場合にはこの悪い細菌を殺す抗生剤を使うと、着床率が元に戻る(上がる)ともいわれています※2。
図1

微量の細菌を調べる ~検査の原理~
ただ、この検査には「限界がある」とか、「あまりあてにならない」という意見もあります※3。そもそもこの検査は、どういう検査なのでしょう?
細菌の検査、というとまず思い浮かぶのは「培養検査」です。かゆみや、「おりもの」が多いときに膣の中の細菌を取って、これを培養して増やし、どういう菌がいるかという検査は外来でよくやられています。
しかし、同じ検査を子宮の中の液でやろうとすると、菌の数が少ないためにほとんど「培養陰性」、つまりばい菌(細菌)はいない、という結果が出ます。そのため、後で述べる次世代シークエンサーが登場する2000年頃まで、子宮の中には原則細菌はいない、と多くの医師が考えていました。
しかし、「PCR」と「次世代シークエンサー」という二つの技術が普及すると、この考えは急速に変わっていきます。PCRはDNAをそのまま何回もコピーして増やす方法です。この方法で数万倍に増やした細菌のDNAを、次世代シークエンサーで解析すると、増幅したDNAの配列を読み取ることができるのです。この二つの技術を組み合わせることによって、どんな細菌がどのくらいいるかを調べることができるようになりました(図2)。
図2

まず、緑色の細菌からDNA(赤)を取り出し、このDNAをPCRで増やします。その後、次世代シークエンサーでDNAの一部の配列を調べます。上段のように配列がAGTCACと最後がCなら乳酸菌、AGTCATと最後がTなら病原菌A、というように見分けがつくわけです。
ここで、DNAのどの部分を読み取るかが問題になりますが、どの細菌も必ず持っていて、異なる細菌では配列が少しだけ違う「16S リボソームRNA」という物質のDNAが、次世代シークエンサーが読み取る対象として設定されました。
16S リボソームRNA
リボソーム(紫色)は、タンパク質を合成するための構造で、バラバラの粒子として(橙色)、あるいは膜構造に接着した形で細胞内に存在します(図3)。
図3
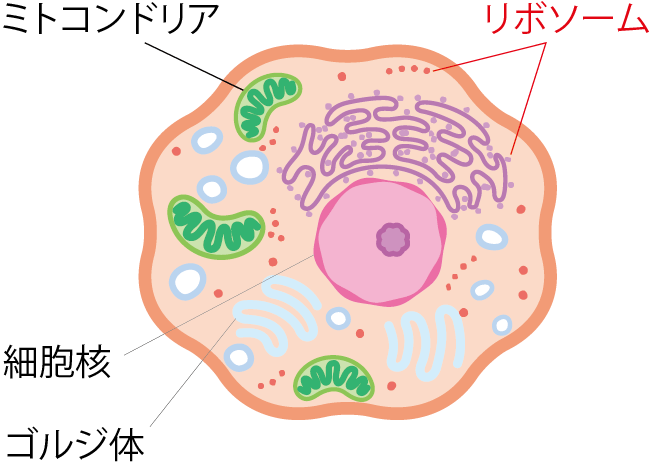
16S リボソームRNAというのは、リボソームの一部を構成する、いわば機械の部品にあたります
(図4)。
リボソームはmRNAの設計図にしたがって、様々なアミノ酸を取り込んで設計図通りにつなげることで、タンパク質を合成します。いわば細胞が生きていくうえで最も重要なタンパク質合成という仕事をしているので、どの細菌も必ず持っています。さらに、タンパク合成を間違いなく、かつ効率よく行うために、できるだけ配列が変わらないようになってるのです。ちょうど故障が少なく、馬力が安定して出るために長い間たくさんの車で愛用されたエンジンの「型式」が、形を変えないで残る、というのと似ています。この「大部分の配列が似ている」ということは、PCRでDNAを増幅するときに絶対必要です。
図4
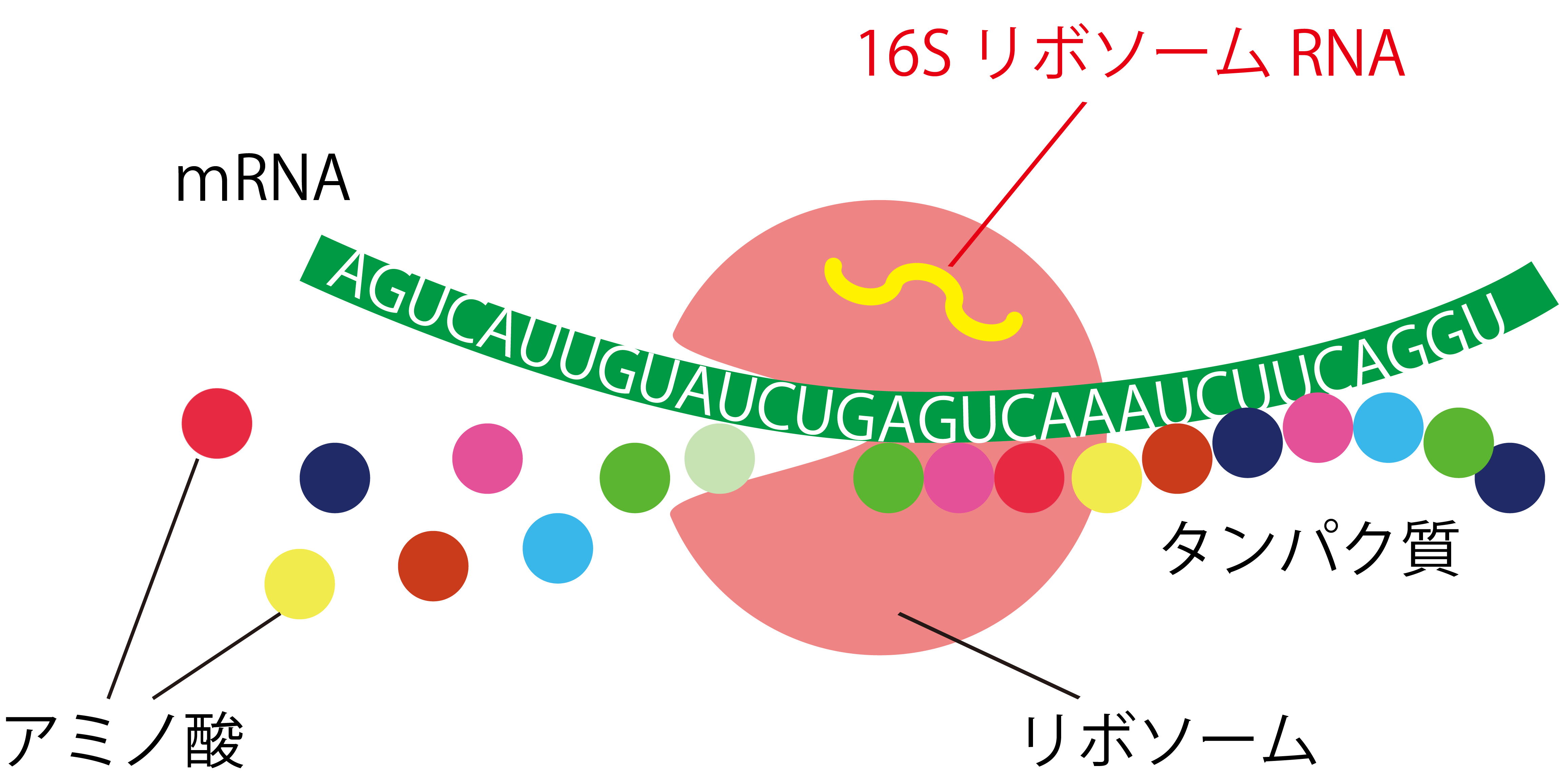
一方、模様替えをしても機能に影響しない部分(「可変部分」)もごく一部に存在するため、16SリボソームRNAのこの部分の遺伝子配列を次世代シークエンサーで解析すれば、どのような細菌かを決定することができるのです。
たとえば、大腸菌はほぼすべての人間が腸の中に持っていますが、その中にO157などひどい病気を起こす特殊な種類の大腸菌もあります。でも通常の大腸菌も、O157も、同じ大腸菌ですから多くの場合、16S リボソームRNAの配列は同じなのです。ということは同じ16S リボソームRNAをもっていても、子宮の中で受精卵が着床する際に悪さをする細菌もいれば、そうでない細菌もいてもおかしくないのです。たとえば、日本人30%、アメリカ人30%、インド人20%、中国人20%という比率の会社が二つあったとして、二つの会社は同じパフォーマンスを出せるでしょうか?
もちろん子宮内細菌叢検査では、そのことは分かっているので、専門家やAIが「このような比率でこの種の細菌が混じっていたら、子宮内の着床環境が確立的に、どのくらい悪くなるかどうか」を細かく計算して予測しています。ただ、この予測の元になるデータは「何回か移植をしたが着床しない、あるいは流産してしまう」方ですので、それ以外の方については間違った答えを出してしまう可能性もあるのです。
結論
結論として、子宮内細菌叢検査は診断と治療に結び付く可能性がある新しい、画期的な検査です。ですが、検査の原理から考えてもまだまだこの検査にはわかっていない点、改良すべき点があり、効果がある患者さんと、効果がはっきりしていない患者さんがいます。反復着床不全など効果がある程度認められている場合はこの検査を使うのは妥当な選択ですが、一般不妊を治療中の方や、はじめて体外受精をする方には原則お勧めできないと、個人的には思います。
リボソームの発見;ジョージ・エミール・パラーデ
さて、今回出てきたリボソームという細胞内の構造(細胞の中にある、決まった働きをする構造;細胞内小器官ともいわれます)が発見されたのは、1950年代です。この発見は何人かの研究者が共同で行ったのですが、その中心となったのはジョージ・エミール・パラーデ(George Emil Palade、1912―2008)(図5)という研究者で、1974年に細胞の構造と機能に関する発見により、クリスチャン・ド・デューブ、アルベルト・クラウデという共同研究者とともにノーベル生理学・医学賞を受賞しています。
パラーデはルーマニア生まれで、ブカレスト大学で医学博士号をとった後1946年、33歳でアメリカに渡り、市民権を得てマンハッタンにあるロックフェラー大学で研究を続けます。彼が初期に用いた研究技術は「細胞分画法」という、細胞を粉々にしたあと、重さによってそれぞれの小器官を分ける方法でしたが、彼がほかの研究者と違ったところは、様々な研究法の長所と短所、限界を冷静・厳密に見定めて、技術を改良できるところはできるだけ改良し、一方で原理的に乗り越えられないところもきちんと把握して、それぞれの持ち味を生かしながら研究を進めたことだと思います。
パラーデがリボソームを電子顕微鏡で発見したのは1958年ですが、彼はその後電子顕微鏡、細胞分画法に加えて放射性物質を合成されているタンパク質に取り込ませる技術などを駆使し、それぞれの技術に新しい改良を加えながら研究をすすめます。最終的には、そのころまだ誰も知らなかった、細胞の中でタンパク質がどこでどのように作られ、最終的にどのように細胞の外に行きつくかの過程を解明し、これがノーベル賞につながるのです。パラーデは1973年に長年勤めたロックフェラー大学からイエール大学に異動し、この大学に初めてできた細胞生物学教室の初代主任教授となっています。研究の詳細は、紙面の関係もありここでは紹介できませんが、タンパク合成におけるリボソーム、ゴルジ体の役割についての彼の発見は60年も前に発見されたにもかかわらず、現在もほぼそのまま通用しています。DNAの二重らせんを発見したワトソン・クリックは誰でも知っていますが、彼の研究はそれに勝るとも劣りません。興味のある方は優れた総説があるので、お時間のあるときにお茶を飲みながら読むにはよいかもしれません。※4
彼のノーベル賞記念講演※5を読むと、研究者がどれだけ多くの可能性を考え、完全ではない実験結果の限界を吟味し、その限界の中に潜む真実を見極めながら一歩一歩研究を進めていったことがよくわかります。暗闇の中たった一人で、小さなろうそくの光を頼りに、時につまずき、しかしつまずいてもただでは起きない確固たる信念のもとに歩みを進め、最終的に果てしない荒野の中の目的地にたどり着くという、まさに研究者にしかできない人生が、この記念講演から伝わってきます。長い英文ですが、たとえ内容は理解できなくても、読む人に本物の研究者の姿が伝わる文章で、一読に値すると思います。
参考文献
※1 Franasiak JM, et al. Endometrial microbiome at the time of embryo transfer: next-generation sequencing of the 16S ribosomal subunit. J Assist Reprod Genet. 2016;33(1):129-36. PMID:26547201
※2 Iwami N, et al. Therapeutic intervention based on gene sequencing analysis of microbial 16S ribosomal RNA of the intrauterine microbiome improves pregnancy outcomes in IVF patients: a prospective cohort study. J Assist Reprod Genet. 2023;40(1):125-135. PMID:36534230
※3 Fasoulakis Z, et al. Impact of the Female Genital Microbiota on Outcomes of Assisted Reproductive Techniques. Biomedicines. 202529;13(6):1332. PMID: 40564051
※4 Zorca SM, Zorca CE. The legacy of a founding father of modern cell biology:
George Emil Palade (1912-2008). Yale J Biol Med. 2011;84(2):113-6. PMID:21698042
※5 https://www.nobelprize.org/prizes/medicine/1974/palade/lecture/




